A betegek számára különösen fontos, hogy orvosuk által javasolt és alkalmazott terápiás eljárás (pl. gyógyszeres kezelés) a legkevésbé kockázatos, ugyanakkor a legnagyobb egészségnyereséggel járjon állapotuk, betegségük eredményes gyógyulása érdekében. (G.S.)
TARTALOM
2. Kutatási elrendezések (típusok)
3. Az orvosi szakirodalomban leírt eredmények értékelése, mérőszámai
Annak érdekében, hogy Ön el tudjon igazodni orvosa által alkalmazott kezelés várható eredményességével kapcsolatban és pontos kérdést tudjon feltenni a várható eredményről, röviden összefoglalom a terápiák értékelhetőségével kapcsolatos általános tudnivalókat. A korszerű prevenció és terápia során figyelembe kell venni, hogy az alkalmazott egészségügyi technológia a legnagyobb egészségnyereséggel járjon, miközben a lehetséges mellékhatásokat minimalizálja.
Nem akkor jó a terápia, ha minél többfélét használunk, hanem akkor, ha a megfelelőt választjuk ki!
Orvosi kérdésekben feltétlenül olyan általános vagy részletes beszámolók az ideális források, amelyek megbízhatók. Ilyenek az elismert orvosi szakfolyóiratok, a szakértők által írt széles körben elterjedt alaptankönyvek, továbbá a nemzeti vagy nemzetközi szakértői testületek által kiadott orvosi protokollok és állásfoglalások, kutatási adatokra történő hivatkozások.
MÉG A SZAKMAI INFORMÁCIÓKKAL IS VIGYÁZNI KELL!
1. A bizonyítékok hierarchiája
Az adatok értékelésének első lépésénél figyelembe kell venni a bizonyítékok hierarchiáját is.
- A hierarchia legalsóbb szintjén a személyes vélemények és bizottsági állásfoglalások helyezkednek el, hiszen ezek hátterében nem feltétlenül áll tudományos igényű megfigyelés.
- Az eset-leírások, esetsorozatok, nem kontrollált klinikai vizsgálatok félrevezetőek lehetnek
- Esetkontroll-vizsgálatok és a kohorsz-vizsgálatok már erősebb bizonyítékokat szolgáltathatnak, azonban ok-okozati összefüggések megerősítésére nem alkalmasak.
- A diagnosztikai vagy terápiás beavatkozások hatásosságának megbízható megítélését a randomizált, kontrollált vizsgálatok szolgáltathatják.
- A bizonyítékok hierarchiájának a csúcsán a több randomizált, kontrollált vizsgálat adatait összegző rendszerezett áttekintő közlemények állnak.

2. Kutatási elrendezések (típusok)
Eset sorozat vizsgálat (case report and series)
Eset sorozat: kontrollcsoport nélküli megfigyeléses vizsgálat, ahol egy gyógyító-megelőző eljárás hatásosságát, mellékhatását, eredményét több eset összegyűjtésével állapítják meg. Hasznos lehet ritka betegségek okának vizsgálatára
Keresztmetszeti vizsgálat (cross sectional)
Keresztmetszeti vizsgálat: a lakosságot, vagy egy kiválasztott lakossági csoportot egy adott időben vagy időtartam alatt vizsgálja. A kockázati tényezők (expozíció) és a betegségek (nem kívánt eredmény) jelenlétét minden egyes egyénnél, illetve az egyéneken keresztül a teljes populációban, egyidejűleg vizsgálja. Mivel a keresztmetszeti vizsgálatokból OK – OKOZATI ÖSSZEFÜGGÉSEK CSAK FENNTARTÁSOKKAL VONHATÓK LE, ezért általában a keresztmetszeti vizsgálatokat a kockázati tényezők és a betegségek adott időbeni előfordulási gyakoriságának (pont – prevalencia) meghatározására szokták használni. Ezért sokan a keresztmetszeti vizsgálatokat prevalencia vizsgálatnak nevezik.
Az inzulinrezisztencia, a pajzsmirigy hypofunkció és a D-vitamin, a szelén bevitelre vonatkozó ajánlások többnyire ilyen adatokból származnak.
Eset-kontroll vizsgálat (case control studies)
Eset-kontroll vizsgálat: egy olyan ok-okozati összefüggést kereső (retrospektív) vizsgálat, amely során egy már betegségben szenvedő csoportot („eset”) hasonlítanak össze egy jól összevethető referencia („kontroll”) csoporttal. Megvizsgálják, hogy a két csoport milyen mértékben volt kitéve egy bizonyos hatásnak (pl. gyógyszeres kezelésnek), és ebből következtetnek az expozíció (behatás, kezelés) és a betegség között fennálló kapcsolatra.
Kohorsz vagy követéses vizsgálat (cohort studies)
Kohorsz vagy követéses vizsgálat: olyan ok-okozati összefüggést kereső (prospektív vagy retrospektív) vizsgálat, amely során egy bizonyos hatásnak (expozíciónak) kitett csoportot hasonlítanak össze egy expozíciónak ki nem tett csoporttal. A két csoportban összehasonlítják, hogy a követési idő során milyen gyakorisággal lépett fel betegség, majd ebből próbálnak következtetni az expozíció (pl. táplálkozás) és a betegség közötti összefüggésre.
Randomizált kontrollált vizsgálat (RTC)
A résztvevőket két csoportra osztják, az egyik csoportot kiteszik valamilyen beavatkozásnak, míg a másik csoportban nem végzik el az adott beavatkozást. Ezt követően egy meghatározott idő elteltével vizsgálják a beavatkozás következményeként kialakuló valamilyen kimenetelt. A randomizált, kontrollált vizsgálat mindig prospektív vizsgálat, hiszen a vizsgálat tervezése megelőzte a megfigyelni kívánt eseményeket.
Olyan rendszerezett áttekintő közlemény, amely legalább két közlemény adatainak matematikai statisztikai módszerekkel történő egyesítéséből újabb számszerű adatokat állít elő. A meta-analízis célja a statisztikai megbízhatóság növelése azáltal, hogy több tanulmány összevetésével az effektív mintaméret növekszik; az ellentmondó konklúzióra jutó vizsgálatok ellentmondásainak feloldása.
A meta-analízis értékes statisztikai módszer, de hátrányaival tisztában kell lennünk, melyek közül a legfontosabbak:
- a különböző vizsgálatok eltérő tervezése miatt ezeket összevetni, eredményeiket összehasonlítani nehéz és sok hibaforrása van;
- az orvosi irodalomban sokkal gyakoribb a pozitív eredmények leírása, mint a negatívoké, ezért a meta-analízis eredménye könnyen lehet torzított a pozitív eredmények felé.
Szisztematikus irodalmi értékelés
A szisztematikus irodalmi áttekintések olyan transzparens, tudományos módszertannal készülő magas szintű átfogó tanulmányok, amelyek egy adott egészségügyi problémával kapcsolatban összegyűjtik és elemzik az összes létező kutatási eredményt, majd ezek jól meghatározott lépéseken keresztül történő értékelésével (ebben benne van a meta-analízis is) próbálnak választ adni az egészségügyi ellátással kapcsolatos fontos szakmai kérdésekre.
Legmagasabb szintű szisztematikus irodalmi értékeléseket a Cochrane Könyvtár tartalmazza.
A terápiára vonatkozó bizonyítékok forrásai közül tehát a randomizált kontrollált vizsgálatok, azok meta-analízise, illetve a kutatási eredmények szisztematikus értékelése a legfontosabb.

FIGYELEM!
1. Még a randomizált kontrollált tanulmányok (RCT) eredményei is félrevezethetők lehetnek a várható egészségnyereség és a kockázat arányának mérlegelésénél. Az RTC eredménye egy idealizált beteganyagra vonatkozik, szemben a napi gyakorlat során ellátásra kerülő betegekkel. Ezzel magyarázható, hogy egy, a kísérleti (ideális) körülmények között hatásos, illetve hatásosnak leírt terápiás eljárás kevésbé eredményes a napi gyakorlat során.
2. A meta-analízisek vagy a szisztematikus irodalmi értékelések is hordozhatnak buktatókat. Ennek az a magyarázata, hogy a szaklapok sokkal inkább közölnek pozitív, mint negatív eredménnyel záruló tanulmányokat. A meta-analíziseknél az is lényeges, hogy vizsgált populációk között sem epidemiológiai, sem klinikai szempontjából ne legyen igazolható heterogenitás. Ez feltétele annak, hogy a matematikai analízis alapján megbízható gyakorlati következtetéseket tudjunk levonni.
3. A negatív, nem szignifikáns eredménnyel járó tanulmányok gyakran nem kerülnek közlésre és a „szürke irodalom” részét képezik. Előfordulhat az is, hogy csak jelentős időeltolódás után válnak ismertté.
Mindkét publikációs hiba meghamisíthatja a rendszerezett irodalmi áttekintések vagy meta-analízisek végeredményét is . A szürke irodalom feltárására és hatásának tisztázására 2013-ban OPEN projekt (http://www.open-project.eu) keretében tanulmányt végeztek .
Bizonyítékokkal alátámasztott, szisztematikusan kifejlesztett klinikai döntési ajánlások sorozata, amelynek célja, hogy javítsa az egészségügyi ellátás minőségét, hatékonyságát, valamint segítse az orvost és a beteget a legmegfelelőbb ellátás kiválasztásában. Bizonyítékokkal alátámasztott, szisztematikusan kifejlesztett klinikai döntési ajánlások sorozata, amelynek célja, hogy javítsa az egészségügyi ellátás minőségét, hatékonyságát, valamint segítse az orvost és a beteget a legmegfelelőbb ellátás kiválasztásában.
3. Az orvosi szakirodalomban leírt eredmények értékelése, mérőszámai
Az eredmény értékelésénél legfontosabb annak tisztázása , hogy az adott terápiás technológia alkalmazásával milyen mértékű egészségnyereség várható. A klinikai hatás mértékének ismerete azért fontos, hogy annak mértékét, várható esélyét össze lehessen vetni a betegség spontán lefolyásával, illetve az alkalmazás során kialakuló mellékhatás várható mértékével és gyakoriságával.
Az EBM alapú egészségügyi ellátás szempontjából lényeges, hogy a bizonyítékok keresése során talált irodalmi adat betegség, vagy beteg-orientált szempontból (DOE, POEM) vizsgálja az adott problémát. A betegek szempontjából természetesen azok az eredmények fontosak, amelyek egészségükre döntő hatással vannak.
Az alkalmazott terápiás eljárásokat vizsgáló klinikai epidemiológiai kutatások eredményeinek szignifikanciáját - hasonlóan a többi betegséghez és állapothoz - a szövődmények megelőzését, a kezelést vizsgáló kutatásokat, két szinten lehet értékelni:
- Matematikai szignifikancia
- Klinikai szignifikancia
Matematikai szignifikancia
Még a megfelelően kiválasztott statisztika elvégzésénél is előfordulhat olyan matematikailag szignifikáns eredmény (pl. p érték, konfidencia intervallum), ami tévesen kedvező következtetésre ad alapot a terápiájánál, annak ellenére, hogy a vizsgált kezelésnek jelentős klinikailag eredménye nincs.
Ezért a statisztikai szignifikancia mellett a klinikai szignifikanciát, a klinikai fontosságot is figyelembe kell venni, amikor döntünk a legmegfelelőbb terápiáról.
Kutatás során megfogalmazunk egy nullhipotézist H0, ami a kutatási hipotézis ellentéte. A nullhipotézisben azt állítjuk, hogy a vizsgált csoportok között NINCS különbség. (A kutatásiban természetes azt, hogy van, de statisztikailag könnyebb így számolni) Azt a valószínűséget, amely esetén H0-t elvetjük p-vel jelöljük és szignifikanciaszintnek nevezzük.
Leggyakoribb szignifikanciaszint a p<0,05
Konfidencia intervallum (CI) fogalma
A konfidenciaintervallum egy valószínűségi intervallum A konfidenciaintervallum becslést ad egy paraméterre: valószínűleg ezek közé a tartományok közé fog esni. Legtöbbször 95 %-ban adják meg ennek az esélyét. (pl. Ha azt mondjuk, hogy egy gyógyszer szignifikánsan csökkentette a vérnyomást és a csökkenéshez tartozó P érték 0.026, ez kevés támpontot nyújt a hatás megítéléséhez. De ha még hozzátesszük, hogy a vizsgálatban mért csökkenések átlaga 28 Hgmm és az átlag 95%-os konfidenciaintervalluma 20 Hgmm-től 36 Hgmm-ig terjed, akkor ez azt jelenti, hogy a “valódi”, a teljes populációban mért átlag nagy valószínűséggel 20 és 36 között van.)
MEGJEGYZÉS: Soha nem tudjuk a teljes populációt vizsgálni, mindig csak reprezentatív mintából próbálunk következtetni a teljes populációra.
A klinikai szignifikancia azt fejezi ki, hogy a statisztikailag szignifikánsnak talált kutatási eredmény milyen mértékben tekinthető klinikailag is jelentősnek vagy fontosnak. Klinikailag számottevő változásról akkor beszélünk, ha a változás nagysága, azon felül, hogy az eredmény a kontroll csoporthoz képest statisztikailag szignifikáns volt, klinikailag is jelentős (fontos). Vagyis a beteg számára észlelhető és lényegesnek ítélt egészség-nyereséget okoz az új beavatkozás, a jelenlegi rutin terápiához vagy placebóhoz képest. A klinikailag szignifikáns eredményt több paraméterrel lehet értékelni.
RRR, ARR fogalma és szükségessége
Az egyik gyakran használt paraméter az RRR (relatív kockázat csökkenés), ami egy meghatározott esemény (betegség, szövődmény) százalékban megadott gyakoriságának csökkenését adja meg a kezelt csoportban, a kontrollcsoportbeli gyakorisághoz képest.
Önmagában az RRR értéke félrevezető lehet, ezért mindaddig nem értelmezhető, amíg nem ismert, hogy milyen arányban fordul elő a vizsgált esemény a kezeletlen betegeknél, azaz mi a be nem avatkozás kockázata.
Az abszolútkockázat-csökkenés (ARR) egy meghatározott esemény (pl. PCOS-ban kialakuló szövődmény) gyakoriságának különbsége a kezelt és a kontrollcsoport között. Ellentétben a relatívkockázat-csökkenéssel, az ARR képes jelezni a jelentős és a jelentéktelen mértékű változások közötti különbséget.
Például, ha a kontrollcsoportban a mortalitás 12%, a kezelt PCOS csoportban pedig 9%, akkor a relatív kockázat 9/12 vagy 75%, amely 25%-os RRR-nek felel meg, ugyanakkor az ARR csak 3%.
NNT, NNH fogalma és szükségessége
A klinikailag számottevő változás, kockázat közérthető kifejezésére vezették be a number needed to treat (NNT), és a number needed to harm (NNH) kifejezéseket.
Az NNT érték, ami az ARR reciproka, azt fejezi ki, hogy a kontrollhoz képest átlagosan hány beteget kell kezelni egy meghatározott ideig ahhoz, hogy egy bizonyos nem kívánatos eseményt elkerülhessünk (pl. halálesetet, szövődményt, stb.) vagy egy betegnél a kedvező hatást elérjük. Minél kisebb az NNT, annál eredményesebb a kezelés. A gyakorlat számára alkalmazása azért előnyös, mert a kezelendő betegszám, a csoport nagyságának ismerete nélkül is pontosan jelzi a kontrollcsoporthoz viszonyított kezelési eredmény várható gyakoriságát. További előny, hogy a kezelendő betegek száma szoros kapcsolatban van a kontrollkezelésben észlelt kimenetel gyakoriságával is.
Az NNT önmagában nem adja meg azt az időt, ameddig kezelni szükséges a kedvező eredményig, ezért a megfelelő értelmezéséhez mindig szükséges a terápiás időtartam megadása is. Természetesen nem mondja meg az sem, hogy a kezeltek közül ki lesz az az egy, aki elkerüli a nem kívánt eseményt (pl. szívinfarktus). Ennek ellenére az NNT a betegek számára is közérthető módon fejezi ki a kezelés klinikailag is lényeges hatásosságát.
A kutatások túlnyomó többsége sajnos még jelenleg sem adja meg a vizsgált eljárás NNT értékét, hanem leggyakrabban az esélyhányadost (OR)-t számolják ki.
Az NNH azt fejezi ki, hogy a kontroll csoporthoz viszonyítva hány beteget kell egy meghatározott ideig kezelni ahhoz, hogy az adott betegek közül egynél az adott mellékhatás biztosan bekövetkezzen .
Eset-kontroll vizsgálatokban a relatív esély mérésére használt mutató, mely a relatív kockázattal is szorosan összefügg. Megmutatja, hogy a betegségnek hányszor nagyobb az esélye az adott kockázati tényező mellett, mint a kockázati tényező nélkül. Az esélyhányados közelítő becslése a relatív kockázatnak.
Intermedier (köztes) eredmények és kemény végpont (végső eredmény) fogalma
Az eredmények értékelésénél fontos tudni azt is, hogy egy jó vagy rossz laboratóriumi eredmény ÖNMAGÁBAN a betegnek lényegtelen. Tehát a bizonyítékokon alapuló orvoslásban kritikus fontosságú, hogy az adott egészségügyi technológiánál ne a köztes (intermedier) eredmények, hanem a végső eredmények, az úgynevezett kemény végpontok (outcomes, hard end points) legyenek a döntéseknél figyelembe véve. Ezért az alkalmazható terápiák értékelésénél és alkalmazásánál is lényeges szempont, hogy az alkalmazott terápiás technológia hatásosságát, illetve eredményességét milyen szempontból vizsgálták.
A vizsgált változók két fő csoportra oszthatók:
- Intermedier eredmény (pl. inzulin szint)
- Kemény végpont (pl. cukorbetegség, szívinfarktus)
MELYIK A FONTOSABB?
Egy laboratóriumi eredmény?
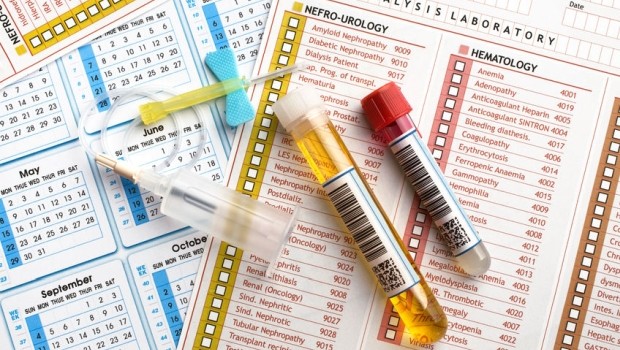
VAGY
A beteg állapota?

(kép forrása: AAPC Knowledge Center)
Az intermedier (pl. labor) eredményt könnyebb mérni, de a rosszul kiválasztott intermedier eredménynél előfordulhat, hogy abból nem lehet következtetni a végső eredményre (pl. késői szövődményre vagy halálozásra).
Tekintettel az intermedier (pl labor eredmény) és a végső eredmény (outcome) közötti nem egyértelmű kapcsolatra, a nőgyógyászati, illetve a nőgyógyászat-endokrinológiai betegségek korszerű terápiájánál és gondozásánál is törekedni kell a végső eredményeket (klinikai tünetek, késői komplikációk, szövődmények, életminőség változás) bemutató kutatások megkeresésére és azok eredményeinek gyakorlati alkalmazására.
Lásd még:
Soroncz-Szabó Tamás: A bizonyítékok és a végpontok hierarchiája. LAM 2001;11(6–7):474–488.
Irodalom
- Gődény S.: A kutatás jelentősége a klinikai hatékonyság megvalósításában. in Gődény S. (szerk): A klinikai hatékonyság fejlesztése az egészségügyben. Pro Die Kiadó , Budapest, 2007,337-386. (ISBN: 978 963 86914 9 1)
- Gődény S.: Bizonyítékokon alapuló orvosi gyakorlat. In: Gődény S. (szerk): A klinikai hatékonyság fejlesztése az egészségügyben. Pro Die Kiadó, Budapest, 2007, 465-506. (ISBN: 978 963 86914 9 1)
- Gődény S., Kardos L.: A klinikai epidemiológiai kutatások tervezésének és értékelésének fő lépései. In: Gődény S. (szerk): A klinikai hatékonyság fejlesztése az egészségügyben. Pro Die Kiadó , Budapest, 2007, 829-867. (ISBN: 978 963 86914 9 1)
- Mogyorósy Zsolt, Bereczki Dániel: Irodalomkutatás és a szakirodalom kritikus értékelése. In: Gődény S. (szerk): A klinikai hatékonyság fejlesztése az egészségügyben. Pro Die Kiadó , Budapest, 2007, 284-338. (ISBN: 978 963 86914 9 1)
Szeretne megoldást találni nőgyógyászati és endokrinológia panaszaival kapcsolatban? Szeretne javítani hormonegyensúlyán és egészségén?
Az alábbi problémákra nálam megnyugtató szakértői segítséget kap!
Nőgyógyászati panaszok • PCOS • Inzulinrezisztencia • Fokozott szőrnövekedés, pattanások • Elhízás • Meddőség • Pajzsmirigy- és mellékvese rendellenességek • Egyéb hormonális problémák.
Kattintson az alábbi lehetőségek egyikére.

.jpg)
.jpg)

.jpg)


.jpg)